Ատոմը կազմված է՝ էլեկտրոններից, նեյտրոններից և պրոտոններից։
Այդ ուղղությամբ առաջին հայտնագործությունը կատարեց անգլիացի գիտնական Ջ. Թոմսոնը:
1898 թվականին նա հայտնաբերեց ատոմի կազմի մեջ մտնող և տարրական լիցք կրող փոքրագույն մասնիկը՝ էլեկտրոնը:
Այդ ուղղությամբ առաջին հայտնագործությունը կատարեց անգլիացի գիտնական Ջ. Թոմսոնը:
Էլեկտրոնի լիցքը՝ qe=−e=−1,6⋅10−19Կլ , իսկ զանգվածը՝ me=9.1⋅10−31կգ
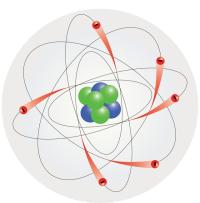 Էլեկտրոնը անհնար է զատել իր լիցքից, որը միշտ միևնույն արժեքն ունի: Տարբեր քիմիական տարրերի ատոմներում պարունակվում են տարբեր թվով էլեկտրոններ: Շարունակելով ատոմի կառուցվածքի բացահայտման հատուկ փորձերը, անգլիացի գիտնական Էռնեստ Ռեզերֆորդը 1911
Էլեկտրոնը անհնար է զատել իր լիցքից, որը միշտ միևնույն արժեքն ունի: Տարբեր քիմիական տարրերի ատոմներում պարունակվում են տարբեր թվով էլեկտրոններ: Շարունակելով ատոմի կառուցվածքի բացահայտման հատուկ փորձերը, անգլիացի գիտնական Էռնեստ Ռեզերֆորդը 1911
Էլեկտրոնները շարժվում են արագացմամբ, որի պատճառը միջուկի և Էլեկտրոնի փոխադարձ ձգողությունն է: Էլեկտրոնի և միջուկի գրավիտացիոն փոխազդեցությունը շատ փոքր է` մոտ 10−40ն , հետևաբար նրանց փոխազդեցությունը հիմնականում էլեկտրամագնիսական բնույթի է:
Սովորական վիճակում մարմինը, ինչպես և նրա կառուցվածքային տարրերը՝ ատոմները, էլեկտրաչեզոք են: Ուրեմն վերջինիս բոլոր էլեկտրոնների գումարային լիցքի բացարձակ արժեքը հավասար է միջուկի լիցքին:
Տարբեր տարրերի ատոմները միմյանցից տարբերվում են իրենց միջուկի լիցքով և այդ միջուկի շուրջը պտտվող Էլեկտրոնների թվով:
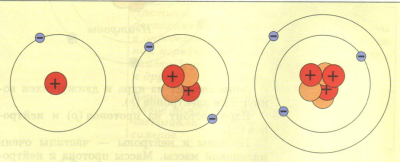
Դ. Ի. Մենդելեևի քիմիական տարրերի պարբերական աղյուսակում տարրերի կարգաթիվը՝ Z -ը, համընկնում է սովորական վիճակում տվյալ տարրերի ատոմի մեջ պարունակվող էլեկտրոննեի թվի հետ, հետևաբար էլեկտրոնների գումարային լիցքը ատոմում հավասար է՝
Միջուկի լիցքը կլինի՝
Ատոմի միջուկը ևս բարդ կառուցվածք ունի. նրա կազմության մեջ մտնում են տարրական դրական լիցք կրող մարմիններ՝ պրոտոններ:
qp=e=1,6⋅10−19կլ
Պրոտոնի զանգվածը մոտ 1840 անգամ մեծ է էլեկտրոնի զանգվածից: Դատելով միջուկի լիցքից կարելի է պնդել.
Ատոմի միջուկում պրոտոնների թիվը հավասար է տվյալ քիմիական տարրի կարգահամարին՝ Z -ին:
Ինչպես ցույց տվեցին հետազոտությունները, բացի պրոտոններից միջուկի պարունակում է նաև չեզոք մասնիկներ, որոնց անվանում են նեյտրոններ:
Նեյտրոնի զանգվածը փոքր ինչ մեծ է պրոտոնի զանգվածից: Նեյտրոնների թիվը միջուկում նշանակում են N տառով:
Միջուկի պրոտոնների՝ Z թվի և նեյտրոնների N թվի գումարին անվանում են միջուկի զանգվածային թիվ և նշանակում A տառով:
 Այսպիսով, ատոմի կենտրոնում դրական լիցք ունեցող միջուկն է, որը կազմված է
Այսպիսով, ատոմի կենտրոնում դրական լիցք ունեցող միջուկն է, որը կազմված է
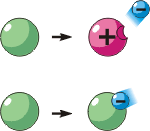
Որոշ դեպքերում ատոմները կարող են կորցնել մեկ կամ մի քանի էլեկտրոններ: Այդպիսի ատոմն այլևս չեզոք չէ, այն ունի դրական լիցք և կոչվում է դրական իոն: Հակառակ դեպքում, երբ ատոմին միանում է մեկ կամ մի քանի էլեկտրոն, ատոմը ձեռք է բերում բացասական լիցք և վեր է ածվում բացասական իոնի:

No comments:
Post a Comment